Усі ці сполуки належать до класу солей.
Солі — це складні речовини, що містять катіони металічних елементів та аніони кислотних залишків.
У формулах солей на першому місці пишуть символ металічного елемента, а потім кислотний залишок:

Таблиця 5
Кислотні залишки
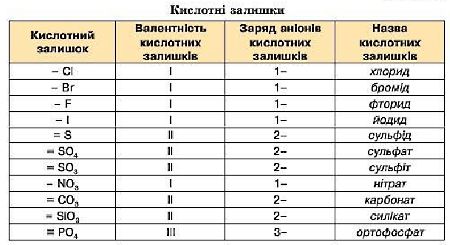
Назви солей складаються:
• для елементів зі сталою валентністю:

• для елементів зі змінною валентністю:
наприклад: FeSO4 — ферум (ІІ) сульфат, CuCl2 — купрум (ІІ) хлорид.
наприклад: K2SO3 — калій сульфіт, CaCO3 — кальцій карбонат;
Формули солей складають аналогічно формулам оксидів, зрівнюючи заряди атомів металічного елемента й кислотного залишку.
Алгоритм складання формул солей
(на прикладі натрій ортофосфату та алюміній силікату)
Деякі солі, що широко використовуються в побуті, крім наукових, мають побутові (традиційні) назви. Наприклад, ви вже знаєте, що натрій хлорид NaCl називають кухонною або кам’яною сіллю, натрій карбонат Na2CO3 — це кальцинована сода, калій карбонат K2CO3 — поташ. Традиційні назви найбільш уживаних солей наведено в опорній схемі.
Поширення солей у природі
У природі солі є основною складовою більшості мінералів. Кухонна сіль — галіт; кальцій карбонат — мармур, вапняк, крейда; кальцій сульфат CaSO4 — гіпс та інші.
Солі відіграють важливу роль у процесах обміну речовин у живих організмах. Вони обов’язково присутні в м’язах, кістковій та нервовій тканинах. Наприклад, солі Калію відповідають за роботу серцевого м’яза. Натрію — за передавання нервового сигналу, завдяки чому організм сприймає інформацію ззовні та реагує на неї. Для росту кісток і зубів необхідні солі Кальцію.
Солі розчинені у клітинному сокові рослин. Недостатня кількість солей у ґрунтах знижує врожайність культур, тому сільське господарство використовує певні солі як мінеральні добрива.
Фізичні властивості солей
Солі — йонні сполуки. За звичайних умов це тверді речовини, з високими температурами плавлення та кипіння. Солі переважно безбарвні, або, як кажуть, білі. Це, наприклад, хлориди та сульфати Калію, Натрію,
Магнію, Цинку й інші. Деякі можуть бути забарвлені в різні кольори та відтінки: купрум(ІІ) сульфід CuS — чорний; нікель(ІІ) сульфат NiSO4 — зелений; кобальт(ІІ) сульфат CoSO4 — рожевий.
Розчинність є важливою характеристикою солей, вона дуже різноманітна. Є солі розчинні, малорозчинні та практично нерозчинні у воді. Наприклад, усі солі Натрію та Калію, а також усі нітрати добре розчинні. Серед силікатів, карбонатів, сульфітів, фосфатів і суль-
фідів переважна більшість солей — нерозчинні у воді, наприклад: FeSiO3, CrPO4.
Встановити розчинність солей у воді можна за Таблицею розчинності.
Таблиця розчинності основ, кислот, амфотерних гідроксидів і солей у воді за температури 20—25 0C
Смак не є фізичною властивістю, і кожен знає, що речовини на смак у лабораторії пробувати не можна. Відомо, що алхіміки, досліджуючи властивості речовин, випробували їх на смак. Інколи це закінчувалось трагічно. Все ж встановлено, що серед солей солоний смак мають лише кухонна сіль, калій хлорид і натрій сульфат, інші — гіркі або змішаних смаків. Солодкими на смак є солі Берилію та Плюмбуму, але ці солі отруйні.